
发布日期:2021.07.27
疫苗接种被认为是新型冠状病毒对策的支柱,并且需要一种银弹才能结束,但治疗剂的发展并没有像我预期的那样发展。近来,新型冠状病毒感染症的治疗药物的开发取得了进展,从轻度到重症都能对应的药物逐渐备齐。截至今年7月中旬,国内已批准4种新型冠状病毒治疗药物。此外,一些正在开发中的治疗药物将争取在年内获得批准。
中外制药公司生产的“罗纳普利布静脉滴注组合300”和“该组合1332” (通用名称:Cacilivimab和Imbivimab) 可用于轻度感染的药物,约占新冠病毒感染的80%。今年7月19日得到了厚生劳动省的特例承认。作为从一开始就以治疗新型冠状病毒为目的而开发的药物,是国内第一个。该药物同时滴注两种病毒中和抗体:卡利比单抗和伊姆比单抗。新型冠状病毒可以与人体细胞结合,进入人体并繁殖,这种治疗被称为“抗体鸡尾酒疗法”,通过两种不同类型的抗体与病毒结合,阻止病毒进入人体。其结果是防止病毒的繁殖,减轻重症化的风险。受试者是患有严重危险因素的轻度至中度住院患者,如年龄,肥胖,潜在疾病,不需要氧气。与非给药组相比,国外临床试验可将住院或死亡风险降低约70%。此外,非临床试验证实它对多种突变株有效,包括Delta菌株。去年美国前总统唐纳德•特朗普 (Donald Trump) 感染新冠病毒时,该药物曾被使用,并引发热议。
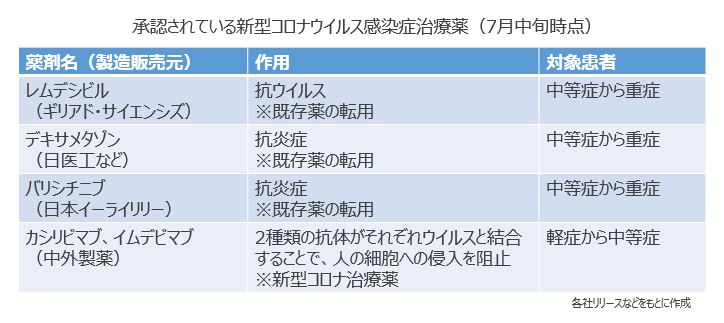
有三种药物被批准用于治疗中重度新冠肺炎,其中许多药物已被转用,用于治疗其他疾病。吉利阿德・赛恩斯的雷姆德西韦是作为埃博拉出血热的治疗药而开发的, 2020年5月被特别批准用于重症患者,今年1月也可用于中等症患者。在临床试验中,从给药开始到第14天恢复的患者比例在Remdivir组为74.4%,在标准治疗组为59.0%。另外,14日时的死亡率,利木地韦组为7.6%,标准治疗组为12.5%。日医工等作为后发品制造的地塞米松是作为重症感染症和间质性肺炎等的治疗药被认可的类固醇药物,去年7月以中等症到重症的患者为对象,在没有审查・认可的情况下被认定。在英国的临床研究中,需要呼吸机的患者的死亡率在标准治疗组中约为40%,而在地塞米松组中约为29%。日本礼来的Valicinib是一种治疗类风湿性关节炎的药物,通过抑制与炎症反应相关的JAK (Janus激酶) 酶来抑制症状。今年4月以中等症到重症的患者为对象被特别批准了。新型冠状病毒严重时会产生过度免疫反应,导致器官损害,但该药具有抑制免疫异常引起的炎症的作用。
此外,多家国内企业正在争取年内批准候选治疗药物。中外制药开发的风湿性关节炎药物阿克拉霉素今年6月从美国食品药品管理局 (FDA) 获得了使用人工呼吸器和ECMO (体外膜式氧合器) 等治疗重症患者冠状病毒的紧急使用许可。日本国内已经完成了临床试验,将在年内进行认可申请。该药物具有抑制过度免疫反应的作用,并且在英国的临床试验中发现可以降低死亡风险。富士胶片富山化学于去年秋天申请批准Abigan,一种开发的抗流感药物,但由于临床试验方法的问题,“难以判断有效性”等。继续审议。为此,将重新以重症化风险高的50岁以上的患者为对象实施临床试验,预定在今年秋天之前完成。兴和表示,对于已经确认具有抑制新型冠状病毒增殖效果和抗炎症作用的抗寄生虫药伊维菌素,将在日本国内进行以轻症患者为对象的临床试验,争取在年内获得批准。此外, 7月26日, Shionogi Pharmaceutical宣布开始对口服剂型的新型冠状病毒治疗药物进行临床试验 (临床试验) 。该药物通过选择性抑制3CL蛋白酶 (一种新冠病毒生长所必需的酶) 来抑制冠状病毒的生长。临床试验预定以健康人为对象进行给药,验证安全性等。第二阶段以后的临床试验和认可申请的时间尚未确定。
MEDIUS Group 正在发展以销售医疗设备为中心的业务。参与医疗的我们(Medical + us)也想扮演一个信息源(Media)的角色,为医疗领域和人们明天的健康提供有用的信息。